-
A meta é aplicar a 1ª dose em todos os paulistas com mais de 18 anos até 15 de setembro.
-
Reconhecimento de 'boas práticas de fabricação' é exigido para que imunizante seja distribuído no País.
-

A previsão para que o primeiro lote da vacina russa chegue ao Brasil até a próxima semana.
-
-
O estudo clínico do imunizante deve reunir 150 voluntários e vai ser conduzido em quatro Estados.
-

Imunizantes chegaram entre os dias 25 e 26 de junho, mas ainda não foram aplicados na população.
-

Segundo a Anvisa, uma das informações faltantes se refere à inativação do vírus utilizado no imunizante.
-
-

Agência alegou ‘falta de alinhamento’ entre fabricante e empresa que protocolou o pedido de autorização.
-
Pesquisadores vão avaliar a segurança, resposta imune e eficácia de proteção do imunizante.
-
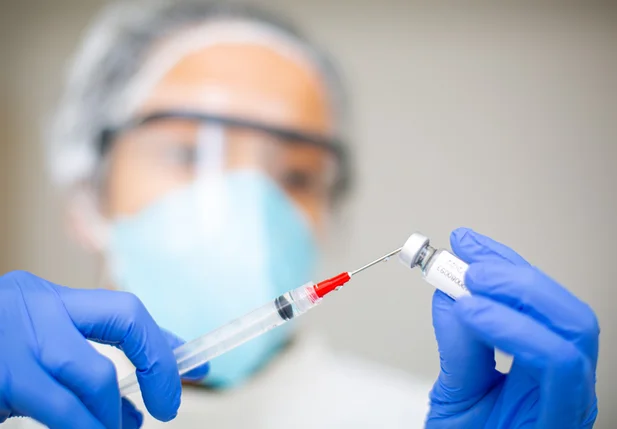
As 3 milhões de doses fazem parte de um total de 38 milhões de doses compradas pelo Governo Federal.
-
-
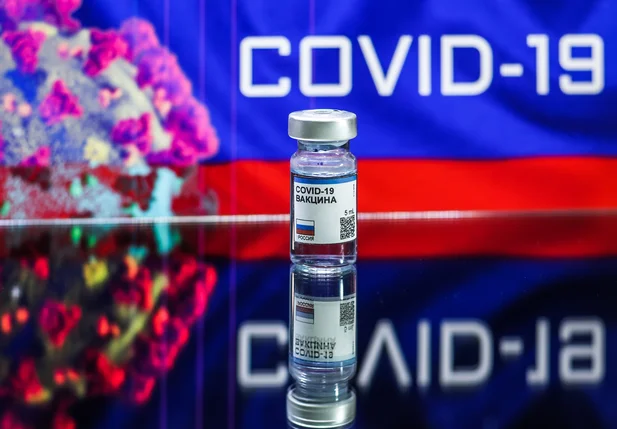
Imunizante poderá ser aplicado apenas em adultos, sem comorbidades e ainda não vacinados.
-
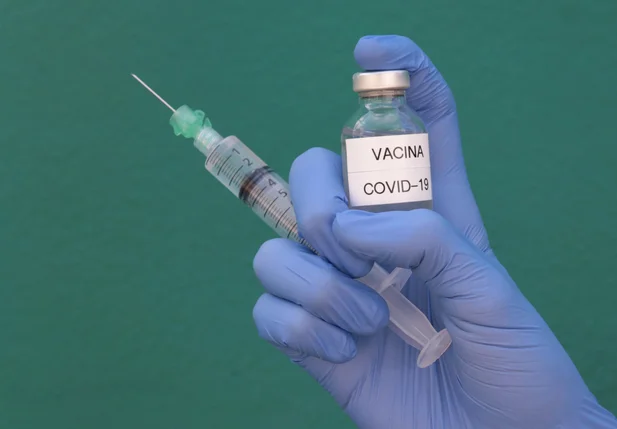
O pedido para a extensão no prazo de validade do imunizante já havia sido apresentado pela Janssen.
-
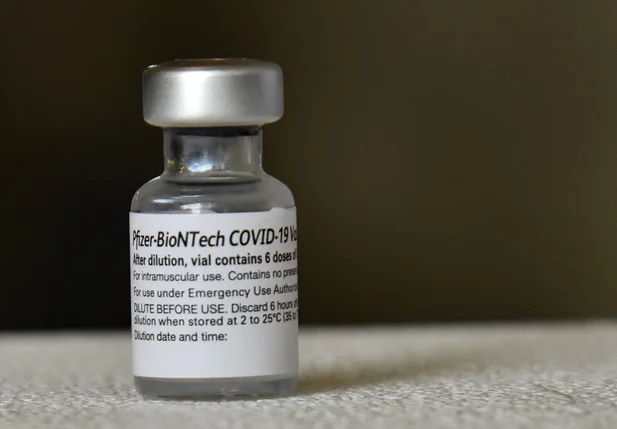
Com a decisão, a bula da vacina passará a indicar esta nova faixa etária para o Brasil.
-
-

De acordo com Wellington Dias, o município escolhido vai ter sua população entre 18 e 60 anos imunizada.
-

A diretoria estabeleceu limitações para o uso desses imunizantes contra a covid-19 no Brasil.
-
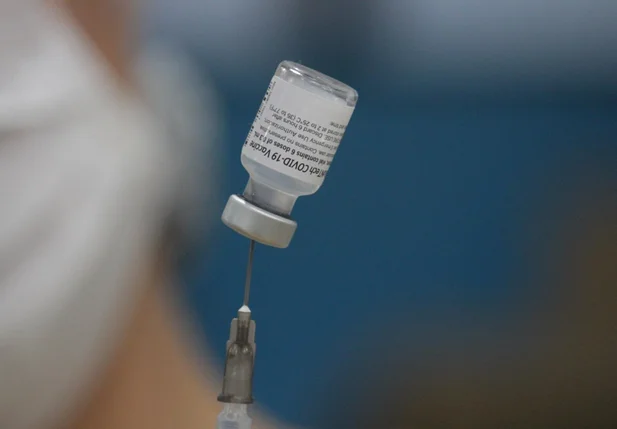
Pedidos pela Agência Nacional de Vigilância Sanitária serão avaliados em reunião extraordinária às 14h.
-
-
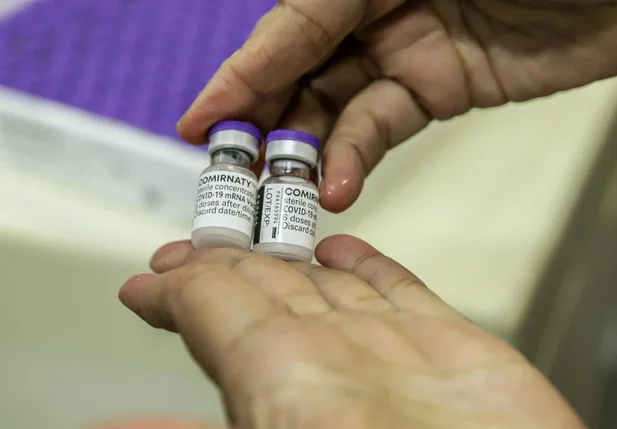
Autorização já foi concedida por agências regulatórias do Canadá e dos Estados Unidos.
-

O paciente tem 32 anos, é morador de Campos dos Goytacazes, no Rio de Janeiro.
-

O soro é desenvolvido pelo Instituto Butantan a partir do plasma de cavalos.
-
-

Agência Nacional de Vigilância Sanitária havia rejeitado a primeira solicitação em março.
-
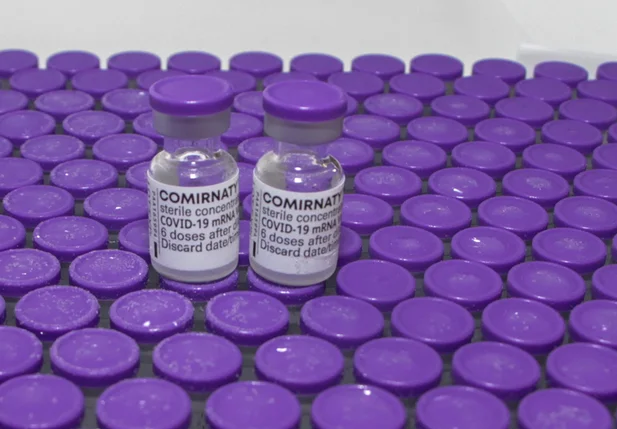
A autorização já foi concedida por agências regulatórias dos Estados Unidos e da União Europeia.
-

O imunizante analisado é oferecido em apenas uma dose. A agência tem sete dias úteis para se manifestar.
-
-
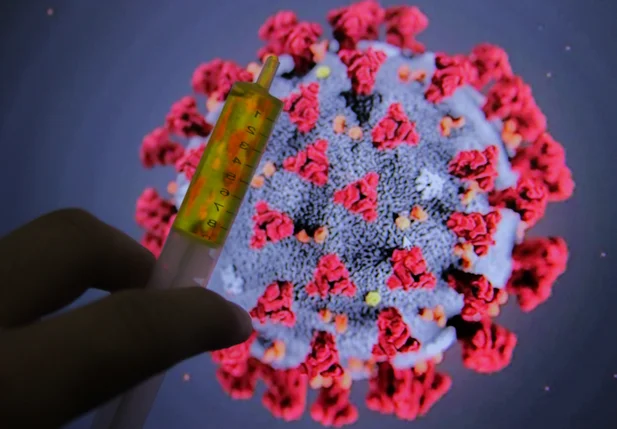
Os medicamentos são indicados logo após a identificação do coronavírus no corpo do paciente.
-
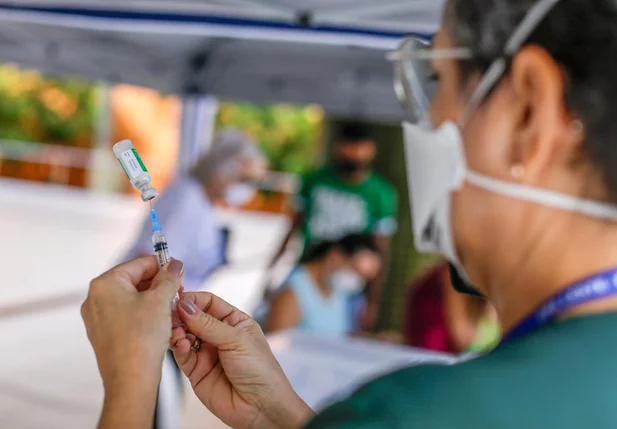
A orientação da Anvisa é para que seja seguida a bula atual do medicamento da AstraZeneca.
-

A Agência Nacional de Vigilância Sanitária atendeu a decisão do ministro Ricardo Lewandowski do STF.
-
-
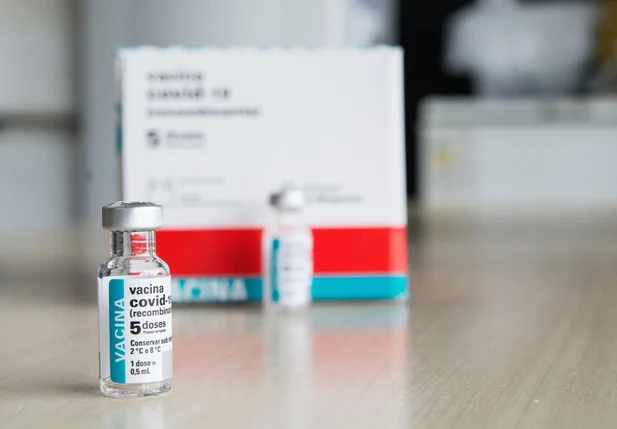
A orientação pede que seja seguida a bula do imunizante, que não consta o estudo no uso de gestantes.
-

Orientação da agência é que seja seguida a bula do imunizante, que não consta a aplicação em gestantes.
-

O governador Flávio Dino acionou o STF alegando que deve ocorrer reavaliação para compra do imunizante.
-
-

Após testes, a Fiocruz vai pedir à Anvisa o registro ou uma autorização para uso emergencial da vacina.
-

Os dados que contribuíram para a negativa foram baseados em informações repassadas pelos próprios russos.
-

O presidente da Anvisa também foi convocado para prestar depoimento na próxima semana.
-
-

Estados como a Bahia e Maranhão pretendem solicitar nova análise.
-
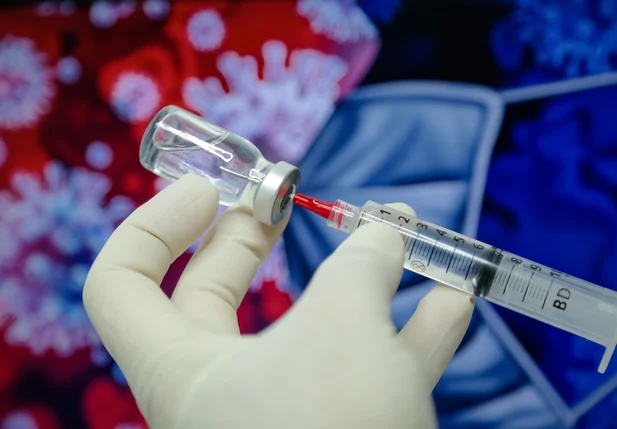
Especialistas dizem que agência acertou diante da falta de dados sobre imunizante russo contra a covid-19
-

Agência regulatória identificou problemas nos estudos clínicos e no processo produtivo do imunizante.
-
-
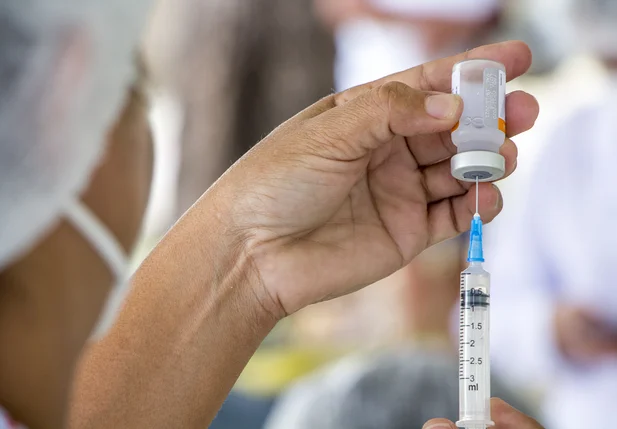
Dados preliminares apontam que imunizante da Índia protege 100% contra casos graves.
-
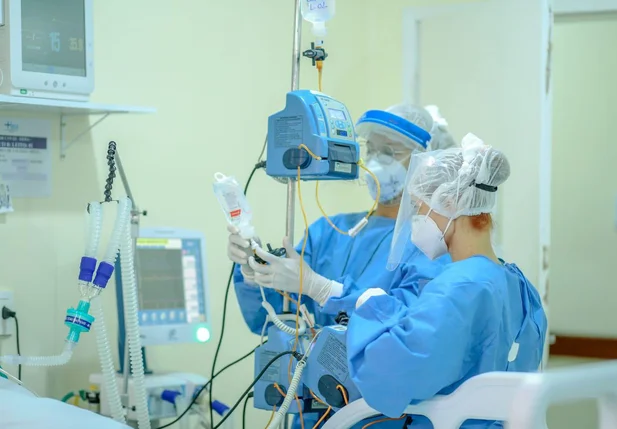
O uso do medicamento vai ser restrito a hospitais, com venda proibida no comércio e farmácias.
-

O imunizante é desenvolvido pela farmacêutica chinesa Sichuan Clover.
-
-

Municípios afirmaram ter recebido ampolas com quantia inferior à informada.
-

"Ela é importantíssima para o momento do Brasil, uma vacina que já foi comprovada", afirmou o governador.
-

Os resultados da fase 3 de pesquisa desse coquetel foram divulgados nesta segunda-feira, 12.
-
-

O imunizante ainda não foi aprovado pela Anvisa e o órgãos pede relatórios de países que usam a Sputnik.
Mais Assuntos
Encontre em ordem alfabética
© 2007-2024 GP1 - Todos os direitos reservados.
É proibida a reprodução do conteúdo desta página em qualquer meio de comunicação, eletrônico ou impresso, sem autorização escrita do GP1.




























