O Ministério Público do Estado do Piauí expediu recomendação ao secretário estadual de Saúde, Florentino Neto, e ao presidente da Fundação Municipal de Saúde, Gilberto Albuquerque, para que a aplicação das doses de vacinas contra a covid-19 aconteça respeitando os grupos prioritários preestabelecidos pelo Ministério da Saúde.
A recomendação administrativa 12ª PJ Nº 01/2021 foi assinada pelo promotor de Justiça, Eny Marcos Vieira Pontes, nessa segunda-feira (18). Ela também atinge os presidentes do Conselho Estadual de Saúde do Piauí, Joab Cavalcante Soares, e do Conselho Municipal de Saúde de Teresina, Acilimara Feitosa Moura.

A recomendação, para que os gestores providenciem e acompanhem a aplicação das doses de vacinas contra a covid-19 respeitando os grupos prioritários preestabelecidos pelo Ministério da Saúde, levou em consideração o Informe Técnico "Campanha Nacional de Vacinação contra a COVID-19", elaborado pelo Ministério da Saúde e divulgado ainda na data de ontem, em que são apresentadas as diretrizes e orientações técnicas e operacionais para a estruturação e operacionalização da campanha nacional de vacinação contra a covid-19.
O documento destacou ainda a disponibilidade limitada de doses da vacina, sendo 61.160 para o Piauí, sendo necessária a definição de grupos prioritários para a vacinação, devendo ser priorizados os grupos de maior risco para agravamento e óbito.
Ainda de acordo com o promotor, o referido informe estabelece que "o início da vacinação se dará pelos trabalhadores da saúde, pessoas idosas residentes em instituições de longa permanência (institucionalizadas), pessoas maiores de 18 anos com deficiência residentes em Residências Inclusivas (institucionalizadas) e indígenas vivendo em terras indígenas em conformidade com os cenários de disponibilidade da vacina".
Consta também no informe do Ministério da Saúde que os grupos alvo da campanha são: idosos (60 anos ou mais), indígenas vivendo em terras indígenas, trabalhadores da saúde, povos e comunidades tradicionais ribeirinhas, povos e comunidades tradicionais quilombolas, pessoas com determinadas morbidades, população privada de liberdade, funcionários do sistema de privação de liberdade, pessoas em situação de rua, forças de segurança e salvamento, Forças Armadas, pessoas com deficiência permanente grave, trabalhadores da educação, caminhoneiros, trabalhadores de transporte coletivo rodoviário passageiros urbano e de longo curso, trabalhadores de transporte metroviário e ferroviário, trabalhadores de transporte aéreo, trabalhadores portuários e trabalhadores de transporte aquaviário.
O membro do Ministério Público ressaltou que a ordem dos referidos grupos prioritários deve ser respeitada, uma vez que as doses de vacina são limitadas e devem ser direcionadas para os grupos com mais riscos de desenvolver formas graves da doença.
O promotor concedeu prazo de 05 (cinco) dias, a contar do recebimento da recomendação, para que os destinatários se manifestem acerca do acolhimento da recomendação, informando à promotoria de Justiça, comprovadamente, quais as providências encetadas para seu cumprimento.
Informe Técnico
De acordo com o documento, considerando as duas doses para completar o esquema vacinal (intervalo de 2 a 4 semanas entre elas) e o percentual de perda operacional de 5% estima-se vacinar nesta primeira etapa cerca de 2,8 milhões de pessoas, priorizando os grupos que seguem: trabalhadores da saúde; pessoas idosas residentes em instituições de longa permanência (institucionalizadas); pessoas a partir de 18 anos de idade com deficiência, residentes em Residências Inclusivas (institucionalizadas); e população indígena vivendo em terras indígenas
O informe destacou ainda que diante das doses disponíveis para distribuição inicial aos estados e a estimativa populacional dos trabalhadores de saúde, será necessária uma ordem de priorização desse estrato populacional, recomendando que seja seguida a seguinte ordem para vacinação dos trabalhadores da saúde conforme disponibilidade de doses, sendo facultado a Estados e Municípios a possibilidade de adequar a priorização conforme a realidade local: equipes de vacinação que estiverem inicialmente envolvidas na vacinação dos grupos elencados para as 6 milhões de doses; trabalhadores das Instituições de Longa Permanência de Idosos e de Residências Inclusivas (Serviço de Acolhimento Institucional em Residência Inclusiva para jovens e adultos com deficiência); trabalhadores dos serviços de saúde públicos e privados, tanto da urgência quanto da atenção básica, envolvidos diretamente na atenção/referência para os casos suspeitos e confirmados de covid-19; e demais trabalhadores de saúde.
Clique aqui e confira o informe técnico na íntegra
Distribuição de doses
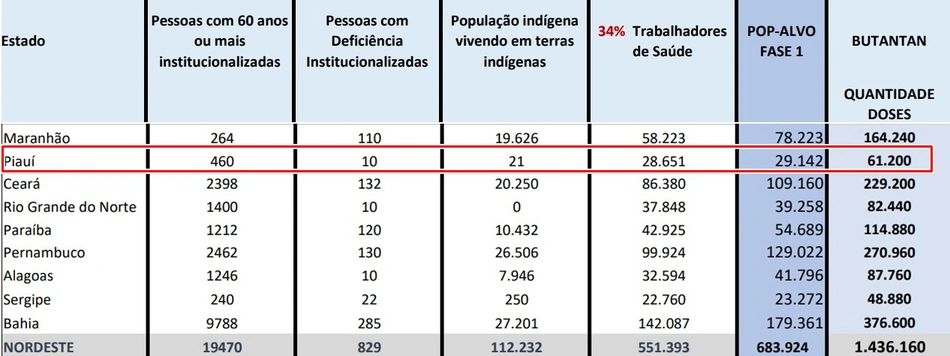
Tabela divulgada pelo Ministério da Saúde mostra a quantidade de pessoas de cada público-alvo que receberá a primeira dose da vacina, em cada estado, nessa primeira fase. No Piauí, serão vacinados 460 idosos em residentes em instituições de longa permanência; 10 pessoas com deficiência institucionalizadas; 21 indígenas e 28.651 trabalhadores da saúde, totalizando 29.142 pessoas.
Uso emergencial
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, por unanimidade, no domingo (17), o uso emergencial da Coronavac e da vacina desenvolvida pela Universidade de Oxford e a farmacêutica AstraZeneca.
A reunião extraordinária que teve início às 10h10 e terminou às 15h20, contou com a votação de cinco diretores: Meiruze Sousa Freitas (relatora); Antonio Barra Torres (diretor-presidente); Cristiane Rose Jourdan Gomes (médica e bacharel em direito); Romison Rodrigues Mota - substituto (servidor da Anvisa); e Alex Machado Campos (advogado).
A diretora da Anvisa e relatora, Meiruze Freitas, votou pela aprovação e destacou que é preciso que o Butantan assine um termo de compromisso para apresentar dados de imunogenicidade da vacina até 28 de fevereiro (os relatórios sobre o tema foram considerados insuficientes). O termo assinado deve ser publicado em Diário Oficial para que a autorização seja válida.
Já a decisão sobre a vacina de Oxford vale apenas para o uso das 2 milhões de doses que o governo ainda tenta importar da Índia. A decisão valeria após a publicação de extrato ou "ciência oficial" via ofício.

 Wanessa Gommes
Wanessa Gommes








Ver todos os comentários | 0 |