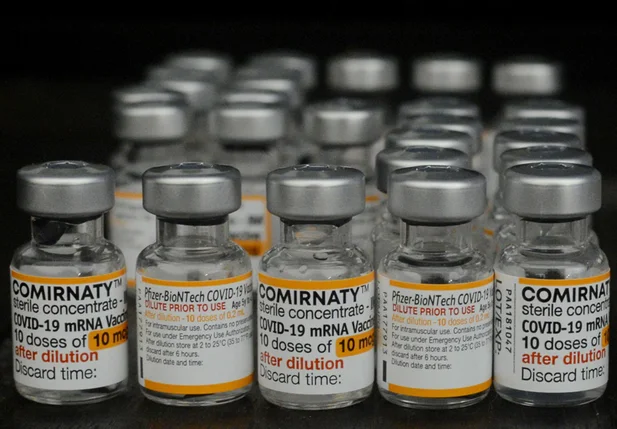-
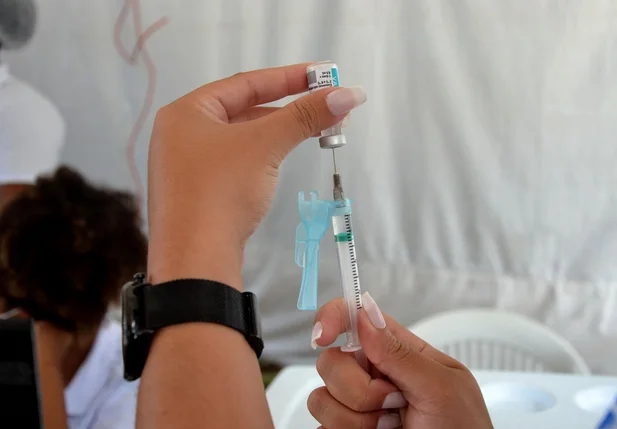
A doença inflama os bronquíolos, estruturas responsáveis por passar o ar das traquéias para os pulmões.
-

O projeto de lei afrouxa a norma que regulamenta o registro de agrotóxicos e vai à sanção presidencial.
-
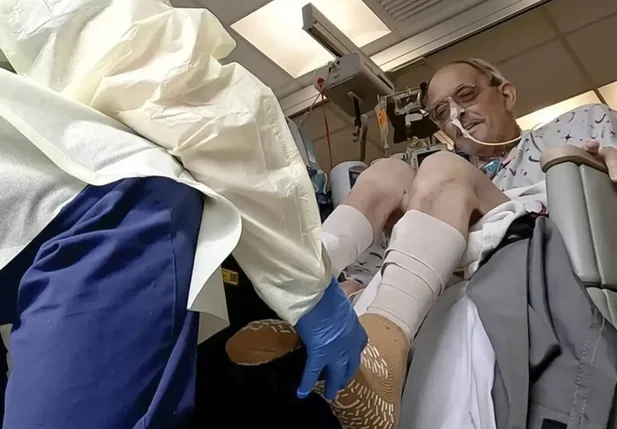
A equipe do hospital divulgou que o coração está funcionando normalmente e sem ajuda mecânica.
-
-

As substâncias presentes nos dispositivos ainda são desconhecidas.
-

Os 28 lotes que estão sendo recolhidos correspondem a 2.237.952 unidades da bebida, sabor maçã.
-

Na última segunda (25), a Anvisa registrou o novo medicamento, que trata-se de uma "caneta injetável".
-
-

Os medicamentos não podem ser considerados intercambiáveis como os similares.
-

Segundo a agência, não há segurança de uso da melatonina presente no suplemento, nessa faixa etária.
-
A lei estabelece que o tratamento com aplicação de ozônio terá caráter apenas complementar.
-
-

Foi proibida a fabricação e comercialização dos produtos das marcas Visipro, Sulinex e Oculares.
-

Testes de HIV, dengue e de colesterol agora poderão ser feitos pelos estabelecimentos.
-

O caso foi julgado na última quinta-feira (25) pela Seção Judiciária de Tubarão, em Santa Catarina.
-
-

Em 2015, última vez que o número de vítimas foi maior, 25 paulistanos morreram com dengue.
-

Haverá um período de transição de 60 dias para conclusão das importações que já estiverem em curso.
-
Trata-se de uma injeção da farmacêutica Novartis, que promete reduzir os riscos de infarto e derrame.
-
-

A vacina foi aprovada em março pela Anvisa e custará até R$ 500, a depender do estado.
-

Ele foi condenado a 6 anos, em regime semiaberto, pelo crime de estupro. A prisão se deu na segunda (12).
-
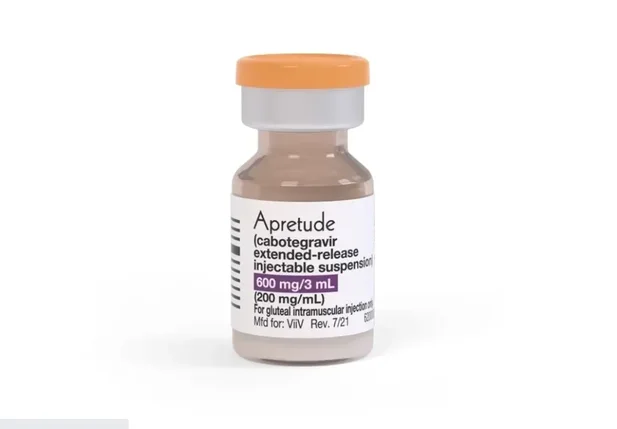
Ele possui uma função de prevenção contra eventuais infecções pelo vírus causador da Aids.
-
-

Os hospitais se destacaram por informar as notificações mensalmente no ano de 2022 à Anvisa.
-

Com a medida da Anvisa publicada hoje, a fabricação de todos os produtos da marca está liberada.
-

A medida já foi comunicada para operadores aeroportuários, postos de fronteira e companhias aéreas.
-
-

Ministério da Saúde fez aquisição emergencial sob o argumento de estoques baixos.
-

A suspensão da comercialização e distribuição será aplicada apenas aos produtos em estoque na empresa.
-
Até 14 de março, 68 pessoas norte-americanos foram diagnosticadas com a bactéria Pseudomonas aeruginosa.
-
-

Anvisa orienta que a população adquira medicamentos apenas em estabelecimentos devidamente regularizados.
-
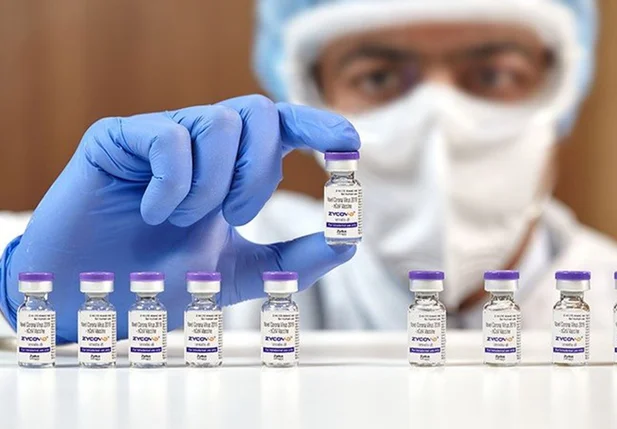
A nova vacina é composta por quatro diferentes sorotipos do vírus, garantindo uma ampla proteção.
-
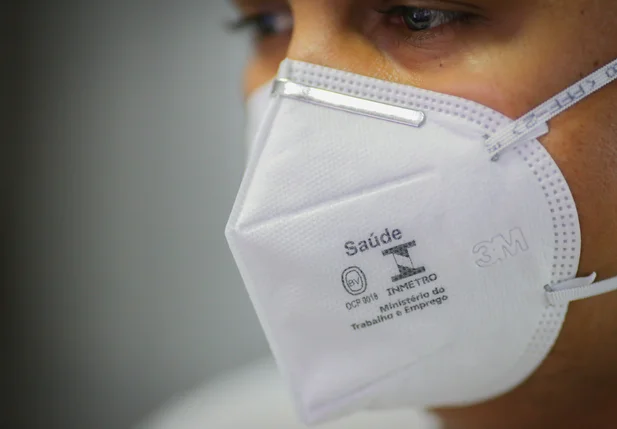
De acordo com a medida, o uso das máscaras passará a ser uma recomendação e não mais uma obrigatoriedade.
-
-

A dose da vacina bivalente é recomendada como dose única de reforço para crianças e adultos.
-

A suspensão dos lotes de camisinhas aconteceu devido falhas no teste que comprova a resistência.
-

O informe é assinado pelo presidente do órgão, José Hiran da Silva Gallo.
-
-

Após relatos de intoxicação ocular, a agência impôs a proibição até a resolução das investigações.
-
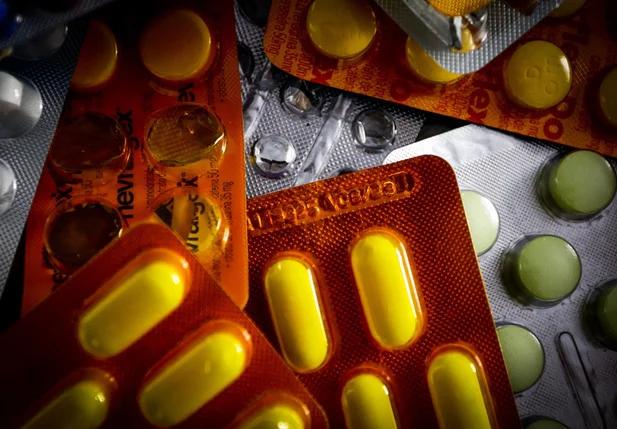
Em abril está previsto reajuste do preço de 10 mil medicamentos, que são regulamentados uma vez por ano.
-
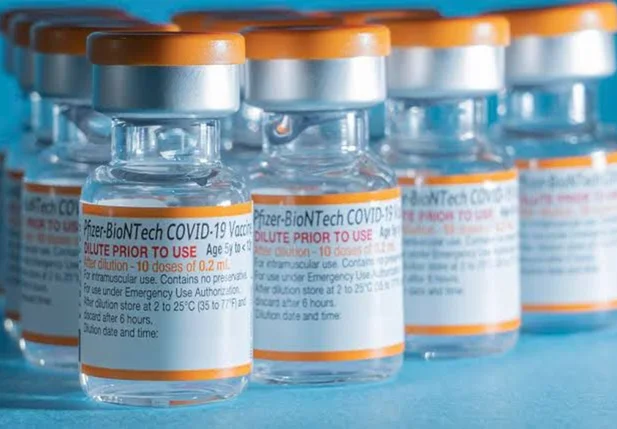
O crescimento é significativo em relação ao ano anterior, já que em 2021 faturou apenas US$ 81,3 bilhões.
-
-

O nutricionista Diego Rocha destacou que os fabricantes utilizam o método para preencher o produto.
-

A semaglutida age na sensação de saciedade, induzindo a perda de peso e a fome dos pacientes.
-

A Agência Nacional de Vigilância Sanitária (Anvisa) alertou que o medicamento não substitui as vacinas.
-
-

A venda do produto será feita em farmácias e drogarias, exclusivamente mediante prescrição médica.
-
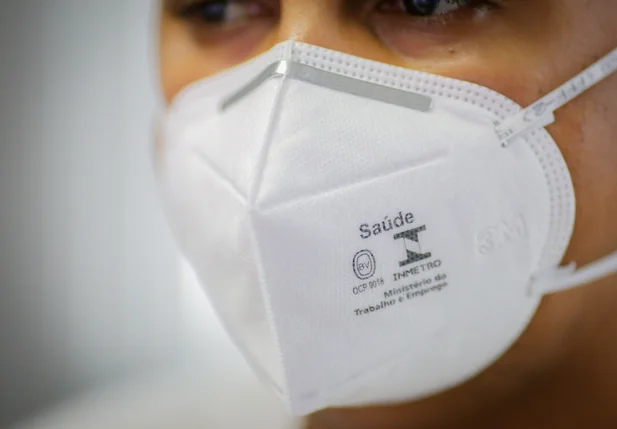
A primeira vez que a obrigatoriedade passou a valer foi em 2020 e permaneceu até 17 de agosto deste ano.
-

A medida passa a valer em todos os aeroportos do território nacional a partir desta sexta-feira, 25.
-
-
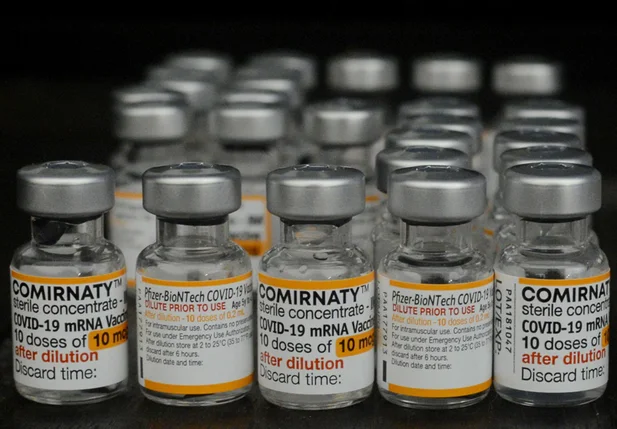
As vacinas bivalentes fazem parte da 2ª geração de imunizantes e protegem.
Mais Assuntos
Encontre em ordem alfabética
© 2007-2026 GP1 - Todos os direitos reservados.
É proibida a reprodução do conteúdo desta página em qualquer meio de comunicação, eletrônico ou impresso, sem autorização escrita do GP1.